体内 (in vivo) CAR-T,为何能成为资本与巨头的必争之地?2026-01-14 13:48:26
近日,双靶点in vivo CAR-T已启动临床研究的原启生物官宣完成7000万美元C1轮融资引起了行业内的热议,聚焦于CAR-T治疗药物的临床进展和转化。
2025年,华中科技大学同济医学院附属协和医院血液科团队在《柳叶刀》发表研究,公布4例复发 / 难治性多发性骨髓瘤患者接受 ESO-T01 载体in vivo CAR-T治疗结果:100%有效,2 例完全缓解,无需清淋预处理,安全性优异。推动国内政策与资本关注。

资本与产业巨头的密集入场,in vivo CAR-T从一开始仅作为“科研热点”,升级为“商业赛道”,这一技术的“横空出世”,正在重新定义细胞治疗的产业格局。
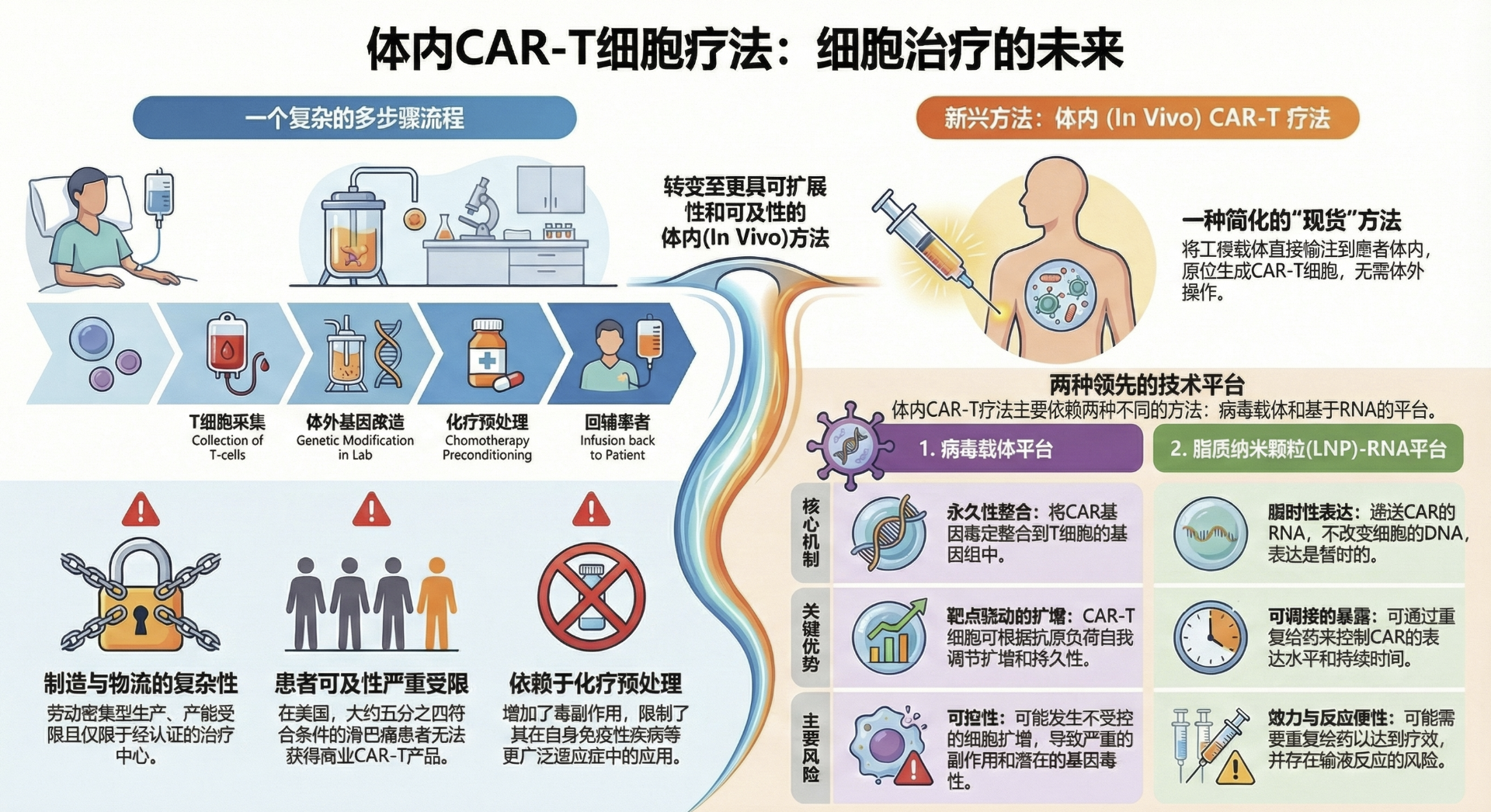
1、传统 CAR-T:体外定制的 “精英疗法”
作用机制:从患者体内抽血分离T细胞,在体外实验室通过基因工程装上 “CAR 导航系统”,扩增后回输体内。
核心短板:流程繁琐(2-4周制备期),病情进展快的患者等不起;成本高昂(单针30-60万元以上),普通患者难以负担;依赖患者自身健康T细胞,高龄、体弱或多次化疗后的患者无法适用;需清淋预处理,存在感染和细胞因子风暴(CRS)风险。
2、in vivo CAR-T:体内生成的 “普惠方案”
作用机制:无需抽血和体外培养,通过静脉注射 “基因递送载体”(慢病毒或LNP脂质纳米颗粒),直接在患者体内将T细胞改造成CAR-T细胞。
核心优势:流程极简(单次注射,当天完成治疗);成本大降(规模化生产后预计降幅 50%-90%,未来或低至万元级);适用人群更广(无需健康 T 细胞,高龄、体弱患者均可耐受);无需清淋预处理,CRS 风险显著降低,安全性更优。
当前,in vivo CAR-T的主流递送策略已分化为两大技术阵营:以慢病毒载体(LVV)为代表的“病毒路径”,和以脂质纳米粒(LNP)为代表的“非病毒路径”。
慢病毒载体:像‘永久植入型快递’,能将CAR基因稳定整合到T细胞基因组,一次治疗可长期起效,但生产工艺较复杂;Interius、Umoja、EsoBiotec等公司是LVV路线的核心玩家。
当前挑战:
1、递送效率仍需提升,确保载体精准靶向T细胞;
2、实体瘤治疗面临肿瘤微环境渗透难题;
3、长期安全性和疗效持久性需更多临床数据验证。
未来方向:
1、AI技术赋能载体设计,提升递送精准度;
2、双靶点、多靶点设计避免肿瘤逃逸;
3、从血液瘤向自免病、实体瘤拓展适应症,打开更广阔市场;
4、病毒载体与非病毒载体技术相互借鉴,平衡安全性与持久性。
需要明确的是,in vivo CAR-T并非要取代传统 CAR-T—— 前者瞄准 “大众可及的普惠治疗”,后者仍会在 “难治性血液瘤的个性化治疗” 中占据一席之地。从体外到体内,CAR-T疗法的进化史,本质是“让精准医疗更普惠”的追求史。当技术突破打破成本与效率的枷锁,细胞治疗将从“小众精英疗法’走向‘大众可及药物”。
